Desde hace tiempo se sabe que todas las moléculas poseen dos cargas iguales y opuestas que están separadas por una cierta distancia. En el caso de tales moléculas polares, el centro de carga negativa no coincide con el centro de carga positiva. El grado de polaridad en tales moléculas covalentes puede describirse mediante el término Momento Dipolar, que es esencialmente la medida de polaridad en un enlace covalente polar.
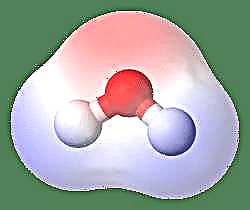
El ejemplo más simple de un dipolo es una molécula de agua. Una molécula de agua es polar debido a la distribución desigual de sus electrones en una estructura "doblada". La molécula de agua forma un ángulo, con átomos de hidrógeno en las puntas y oxígeno en el vértice. Como el oxígeno tiene una electronegatividad más alta que el hidrógeno, el lado de la molécula con el átomo de oxígeno tiene una carga negativa parcial, mientras que el hidrógeno, en el centro, tiene una carga positiva parcial. Debido a esto, la dirección del momento dipolar apunta hacia el oxígeno.
En el lenguaje de la física, el momento dipolar eléctrico es una medida de la separación de las cargas eléctricas positivas y negativas en un sistema de cargas, es decir, una medida de la polaridad general del sistema de carga, es decir, la separación de la carga eléctrica de las moléculas, que conduce a un dipolo. Matemáticamente, y en el caso simple de dos cargas puntuales, una con carga + q y otra con carga? Q, el momento dipolar eléctrico p se puede expresar como: p = qd, donde d es el vector de desplazamiento que apunta desde la carga negativa a La carga positiva. Por lo tanto, el vector de momento dipolar eléctrico p apunta desde la carga negativa a la carga positiva.
Otra forma de verlo es representar el Momento Dipolar con la letra griega m, m = ed, donde e es la carga eléctrica yd es la distancia de separación. Se expresa en las unidades de Debye y se escribe como D (donde 1 Debye = 1 x 10-18e.s.u cm). Un momento dipolar es una cantidad vectorial y, por lo tanto, está representado por una pequeña flecha con una cola en el centro positivo y la cabeza apuntando hacia un centro negativo. En el caso de una molécula de agua, el momento dipolar es 1.85 D, mientras que una molécula de ácido clorhídrico es 1.03 D y se puede representar como:
Hemos escrito muchos artículos sobre el momento dipolar para la revista Space. Aquí hay un artículo sobre de qué está hecha el agua, y aquí hay un artículo sobre moléculas.
Si desea obtener más información sobre el momento dipolar, consulte estos artículos de Hyperphysics and Science Daily.
También hemos grabado un episodio completo de Astronomy Cast sobre Moléculas en el espacio. Escucha aquí, Episodio 116: Moléculas en el espacio.
Fuentes:
http://en.wikipedia.org/wiki/Electric_dipole_moment
http://en.wikipedia.org/wiki/Dipole
http://www.tutorvista.com/content/chemistry/chemistry-iii/chemical-bonding/degree-polarity.php
http://hyperphysics.phy-astr.gsu.edu/hbase/electric/dipole.html#c1
http://en.wikipedia.org/wiki/Water_molecule